Apa Perbedaan Senyawa Ion Dan Senyawa Kovalen

Ketiga jenis senyawa kimia ini tentunya sangatlah penting untuk kita pelajari karena pada materi materi kimia tingkat atas yang akan adik adik pelajari berikutnya akan selalu berkaitan dengan konsep.
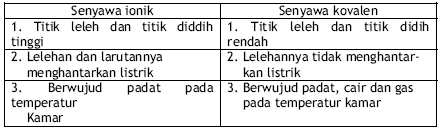
Apa perbedaan senyawa ion dan senyawa kovalen. Contoh logam adalah tembaga seng dan besi sedang non logam contohnya. Senyawa ion itu tidak ada sebagai molekul sehinga kita tidak dapat mengetahui tentang rumus molekul dari senyawa ion. Seperti disebutkan di atas atom perlu membentuk senyawa untuk mencapai konfigurasi elektronik yang stabil. Perbedaan antara senyawa ionik dan senyawa molekul.
Perbedaan ikatan ion dan ikatan kovalen tampak dari atom yang membentuknya. Entalpi fusi energi panas yang diserap bila padat mencair dan entalpi penguapan energi panas yang diserap ketika cairan mendidih lebih tinggi dalam senyawa ion. Perbedaan sifat fisik senyawa kovalen dan senyawa ion senyawa didefinisikan sebagai zat yang mengandung dua atau lebih unsur kimia yang berbeda. Mereka memiliki struktur kimia yang berbeda ditandai dengan rasio tetap atom yang disatukan oleh ikatan kimia.
Apa itu senyawa kovalen. Sebagian besar senyawa kovalen adalah non polar atau memiliki kecenderungan sangat kecil untuk membelah sepenuhnya untuk membentuk ion dan karenanya tidak pernah menghantarkan listrik. Oksigen nitrogen dan karbon. Bagi sebagaian siswa membedakan manakah yang termasuk golongan senyawa ion dan mana yang masuk golongan senyawa kovalen bukan perkara mudah.
Senyawa molekuler lebih mudah terbakar dibandingkan senyawa ion. Pada suhu dan tekanan normal kita akan menemukan senyawa senyawa ini sebagai cairan atau gas. Senyawa kovalen adalah senyawa yang terbentuk dari sesama unsur unsur nonlogam dengan cara membentuk ikatan kovalen penggunaan pasangan elektron bersama. Pada formula atau rumus ionik.
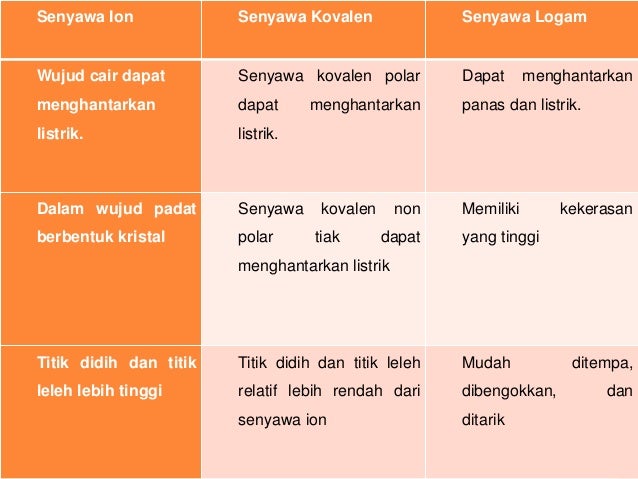
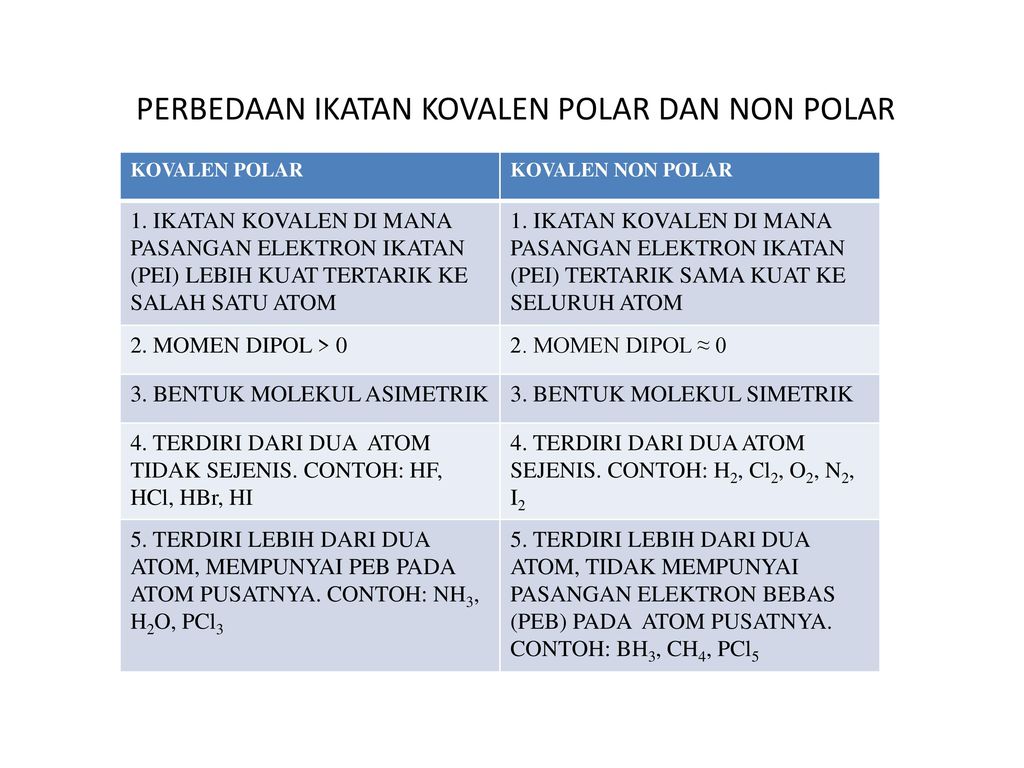
Seperti yang juga adik adik ketahui bahwa senyawa kimia terutama senyawa kimia anorganik itu terdiri dari 3 jenis senyawa yaitu senyawa ion senyawa kovalen polar dan senyawa kovalen non polar. Ikatan kovalen jauh lebih lemah daripada ikatan ion dan oleh karena itu sebagian besar senyawa kovalen ada dalam fase gas. Ini adalah senyawa yang dibentuk oleh atom yang terikat secara kovalen. Ikatan ionik hanya dapat terjadi antara kation dan anion sederhana senyawa ionik hanya dapat terbentuk secara langsung dari ion ion dll.
Ikatan ion adalah ikatan kimia yang terbentuk dari atom logam dengan atom non logam dimana ikatan elektrostatis yang terbentuk antara ion positif dan ion negatif ini akan menyebabkan gaya tarik menarik hingga menghasilkan ion atau senyawa yang dikenal dengan nama senyawa ionik. Sifat elemen ini berbeda dengan sifat pembentuknya membuatnya ini tidak bisa dipisahkan menjadi unsur unsur maupun senyawa yang lebih sederhana melalui reaksi kimia. Senyawa mempunyai sifat yang tidak sama dengan berbagai elemen yang menyusunnya.